国立大学法人千葉大学
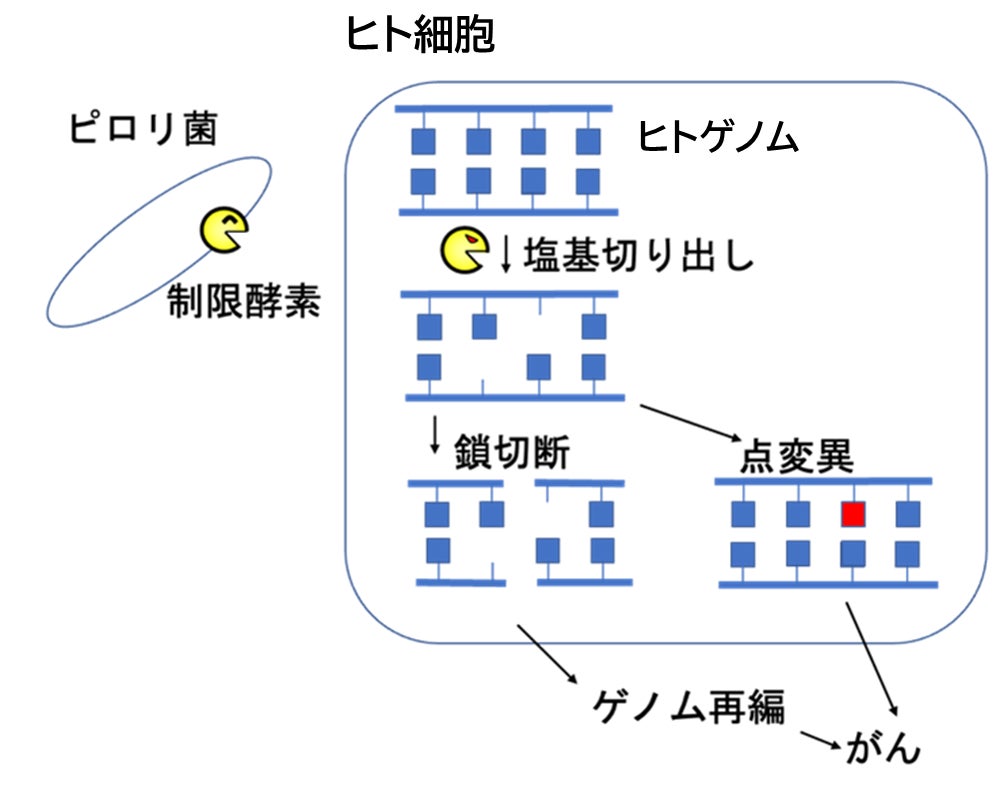
千葉大学大学院医学研究院の福世真樹助教と金田篤志教授は、法政大学マイクロ・ナノテクノロジー研究センターの小林一三客員教授、大分大学医学部の花田克浩講師、杏林大学医学部の大﨑敬子教授らの研究グループと共同で、ピロリ菌の持つ特別な制限酵素(注1)が、ヒトのゲノムに働いて変異と切断を起こし、がんをつくり出すメカニズムを明らかにしました(図1)。胃がんの主な原因はピロリ菌ですが、それがどのようにしてヒトのゲノムに異常をもたらしがんを引き起こすかは不明でした。本研究では、ピロリ菌の持つ特別な制限酵素(DNAを特定の配列で切るハサミ)が、ヒトのゲノムに働いて変異と切断を起こし、がんを創り出す証拠を得ました。これまで知られていなかった新しい発がんメカニズムの提唱であり、今後の胃がんに関する医療の発展が期待されます。
本研究の結果は、2025年8月5日付で国際学術誌PNAS Nexusに掲載されました。
■研究の背景
がんの発症には、これまで遺伝子の変異や生活習慣、環境要因などが深く関わると考えられてきました。しかし近年、ヒトの体内に共生する細菌叢(マイクロバイオーム)が様々な疾患に影響を及ぼすことが分かり、がん研究の新たな焦点となっています。なかでも胃がんは、毎年世界で約100万人が発症し、70万人が命を落とす重大な疾患です。その最大の危険因子はピロリ菌感染であり、これまで cagA 遺伝子など発がんの原因となる因子が報告されてきました。しかし同じ遺伝子型のcagAを持っていても、地域によって発がん率に大きな差があり、従来の説明だけでは不十分でした。そこで注目したのが、ピロリ菌が持つ制限酵素HpPabIです。HpPabIは、DNAの中の特定の塩基の並び(G-T-A-C)を見つけて、そのうちのA(アデニン)という塩基を抜き取るという、通常のDNA二本鎖切断型の制限酵素とは異なり、「塩基切り出し型」という少し変わった制限酵素です。この「抜けた穴」に対し細胞は修復を試みますが、誤った塩基(A以外のT, G, C)を入れて点変異を起こすことがあります。あるいは、DNAの二重らせんが切れてしまい二本鎖切断を引き起こすこともあり、これも誤った修復の原因になります。これらは重大な遺伝子の損傷の原因となります。
■研究の成果
研究グループはまず、がん細胞に蓄積する遺伝子変異のパターン(変異シグネチャー)を解析しました。変異シグネチャーは通常、3塩基の並びについて解析されてきましたが、本研究では4塩基以上の並びについて配列も癌腫も網羅的解析しました。その結果、胃がんで「GTAC」という4塩基の配列の、3番目の「A」で特に変異が起きやすく、ピロリ菌陽性胃がんでは他の全癌腫と比較して約10倍も高頻度に認められました。そこで我々は、GTACのAを切り出すピロリ菌の制限酵素HpPabIに着目しました。世界中の2,300株以上のピロリ菌の遺伝情報を解析し、この酵素を持つ菌株と地域ごとの胃がん発症率を比較したところ、HpPabI遺伝子を持つピロリ菌が、胃がんの発症リスクの増加と相関があることが分かりました。
さらに、培養したヒト細胞にHpPabIを持つピロリ菌を感染させる実験を行ったところ、HpPabIによってDNA二本鎖切断が一定の割合で生じることが確認されました。さらに大腸菌を利用した実験系でも、HpPabIによってゲノムの変異生成が10倍以上高まることが明らかになりました。また立体構造をAI構造予測技術を用いて解析したところ、DNAとの結合や酵素活性に関わる部位に進化の痕跡を見出しました。これらの知見は、HpPabI がヒト細胞のDNAを損傷し、ある部分のDNAが、別のものに置き換わってしまう「点変異」やDNAの二本鎖切断を引き起こすことで、胃がんの発症に関与している可能性を提示するものです。
■今後の展望
今回の研究は、従来の3塩基からなる変異シグネチャーではなく、4塩基以上のDNA配列を用いてがんの遺伝子変異パターンを網羅的に解析することで、これまでになかった全く新しいゲノム変異の特徴を見出し、その配列を認識するピロリ菌の制限酵素 HpPabI が胃がんの新しい発症要因である可能性を提示することに成功しました。これは「感染による炎症」だけでは説明できなかった発がんメカニズムを補うもので、がん研究に新たな視点を与えます。今後は、動物モデルを用いた実験で HpPabI ががんを引き起こすことを示すことが大きな課題です。もし因果関係が明確に示されれば、HpPabI を標的とした新しい診断法や予防法の開発につながる可能性があります。細菌とヒトの遺伝情報の相互作用を解き明かすことは、がんの本質を問い直すと同時に、将来的な個別化医療や新しい治療戦略の基盤となると期待されます。
■用語解説
注1)制限酵素: DNAを特定の配列を認識して切断する、ハサミのような役割を持つ酵素のこと。
■研究プロジェクトについて
本研究は、以下の研究課題の支援を受けて行われました。
・ 日本学術振興会 科学研究費助成事業19K22543(小林一三代表)「ピロリ菌の塩基切り出し型制限酵素は胃がんの原因か?」
・ 日本学術振興会 科学研究費助成事業22K07164(福世真樹代表)「新規変異シグナチャー解析手法による癌変異源の解明」
・ 日本学術振興会 科学研究費助成事業 16H06279「先進ゲノム支援 (PAGS)」
■論文情報
タイトル:Helicobacter pylori base-excision restriction enzyme in stomach carcinogenesis
著者:Masaki Fukuyo, Noriko Takahashi, Katsuhiro Hanada, Ken Ishikawa, Česlovas Venclovas, Koji Yahara, Hideo Yonezawa, Takeshi Terabayashi, Yukako Katsura, Naoki Osada, Atsushi Kaneda, Maria Camargo, Charles Rabkin, Ikuo Uchiyama, Takako Osaki, and Ichizo Kobayashi.
雑誌名:PNAS Nexus
DOI:10.1093/pnasnexus/pgaf244